Природа, морфология и основные свойства бактериофагов. Механизм действия их на бактериальную клетку. Применение их в диагностике, лечении и профилактике болезней
Бактерии, резистентные к большинству или ко всем из всех известных антибиотиков, вызывают всё более серьезные проблемы. Это увеличивает риск возврата человечества к проблемам того периода, когда антибиотики были неизвестны, когда были широко распространены неизлечимые инфекции и эпидемии. Несмотря на интенсивную работу фармацевтических компаний, за последние 30 лет не было найдено новых классов антибиотиков. Есть надежда, что вновь обнаруженная возможность полностью секвенировать микробные геномы и определять молекулярные основы патогенности откроет новые пути лечения инфекционных заболеваний, но с всё большим рвением идет поиск других подходов к этой проблеме. Одним из результатов такого поиска является вновь возникший интерес к возможностям терапевтического использования бактериофагов (от бактерии и греч. phagos — пожиратель; буквально — пожиратели бактерий) - специфических вирусов, которые атакуют только бактерии и убивают патогенные микроорганизмы. Для обозначения фагов вызывающих лизис актиномицетов, применяется термин актинофаг, микобактерий— микофаг, кишечной палочки — колифаг, водорослей — цианофаг и т.д.
Фаговая терапия была впервые разработана в начале этого века и казалась многообещающей, хотя и вызвала много споров. Вначале много внимания уделялось изучению фагов, активных против патогенных бактерий: дизентерийной, брюшнотифозной, дифтерийной палочек, стафилококков с целью выяснения возможности использования их для лечения и профилактики инфекционных заболеваний. Одновременно много внимания уделялось изучению природы фагов. С начала эры антибиотиков в 40-х гг. в западных странах ее использовали мало. Однако в Восточной Европе за последние 50 лет были проведены широкие клинические исследования в отношении фаговой терапии. Результаты этой работы хорошо дополняют ограниченные изыскания последних лет, проведенные на животных на Западе. В последние годы проблема бактериофагии фактически превратилась в самостоятельную область биологии со своими специфическими разделами. Это придает оптимизм в том отношении, что фаги могут, в самом деле, играть важную роль в борьбе с инфекциями, вызываемых микробами, резистентность которых к лекарственным средствам растет.
Фаги оказались весьма удобной моделью для разрешения ряда важнейших теоретических и практических вопросов общей биологии, генетики, молекулярной биологии, биохимии, а также медицины, ветеринарии и вирусологии.
В результате большого теоретического и практического значения проблемы бактериофагии за последние 10—20 лет фаги изучались весьма интенсивно и всесторонне.
История бактериофагов
1896: Эрнест Ханкин сообщил, что воды рек Ганга и Джамна в Индии обладают значительной антибактериальной активностью, которая сохранялась после прохождения через фарфоровый фильтр с порами очень малого размера, но устранялась при кипячении. Наиболее подробно изучал он действие неизвестной субстанции на Vibrio cholerae и предположил, что она ответственна за предупреждение распространения эпидемий холеры, вызванных употреблением воды из этих рек. Однако, в последующем, он не объяснил этот феномен.
1898: Впервые перевиваемый лизис бактерий (сибиреязвенной палочки) наблюдал русский микробиолог Н.Ф. Гамалея.
1915: Английский учёный Ф. Туорт описал это же явление у гнойного стафилококка и открыл первый «вирус, пожирающий бактерии» , когда он наблюдал любопытное дегенеративное изменение - лизис в культурах стафилококков из лимфы теленка. С его именем связано название «феномен Туорта».
1917: Феликс д’Эрель делает аналогичное открытие, Именно Феликс д’Эрель канадский сотрудник Института Пастера в Париже, дал им название “бактериофаги” - используя суффикс “фаг” не в его прямом смысле “есть”, а в смысле развития за счет чего-то (д’Эрель, 1922, р. 21), они стали главной частью работы всей его жизни.
Д’Эрель, микробиолог, преимущественно самоучка, провел 10 лет в Гватемале, Мексике и Аргентине. Там он имел дело с эпидемиями дизентерии, желтой лихорадки и грибков кофейных деревьев, для контроля чумы саранчи он выделил из умирающей саранчи бактерию, а также исследовал несколько интересных загадок брожения. Всё это было хорошей подготовкой к его более поздней работе с фагами и интересно изложено в Summers (1999). В Институте Пастера он проводил кропотливое исследование метода приготовления вакцины с помощью модельной системы - “B. typhimurium” на её природном хозяине мыши, поскольку был твердо убежден в том, что значимые данные об иммунитете и патогенности можно получить только при использовании природных хозяев. В свободное время он также продолжал обследовать дизентерийных больных - частую проблему в воевавшей Франции. Из фекалий нескольких из этих больных он выделил анти-шигелловый “микроорганизм”, который был размножен путем многочисленных серий пассажей на бактерии-хозяине и мог образовывать небольшие чистые круги на газоне этих же бацилл шигеллы (’Эрель, 1917).
Д’Эрель продолжал тщательно характеризовать бактериофаги как вирусы, которые размножаются в бактериях и разрабатывать подробности инфекции различными фагами разнообразных бактерий-хозяев в разных условиях окружающей среды, всегда объединяя в своей работе природные феномены и лабораторные данные, для лучшего понимания иммунитета и естественного (самопроизвольного) излечения от инфекционных заболеваний (Summers, 1999). На Девятнадцатом ежегодном заседании Британской Медицинской Ассоциации в Глазго прошла очень интересная дискуссия между д’Эрель, Twort и несколькими другими выдающимися учеными того времени о природе и свойствах бактериофагов (d'Herelle et al, 1922). Главный её вопрос: является ли причинной основой лизиса бактерий, вырабатываемый ими фермент или это особая форма мельчайшего вируса с некоторым родом собственной жизни, как заявлял д’Эрель. Этот спор продолжался много лет, разделяя людей, работающих с фагами, которых становилось все больше и больше.
Д’Эрель суммировал начальный этап работы с фагами в 300-страничной книге “Бактериофаг” (1922). Он провел классические описания образования бляшек и состава, инфекционных центров, литических процессов, специфической адсорбции на бактерии-хозяина и размножения, зависимости продукции фагов от конкретного состояния бактерии-хозяина, выделения фагов из источников инфекционных бактерий и факторов, регулирующих стабильность внеклеточного фага. Он быстро увлекся очевидной ролью фагов в природном контроле микробных инфекций. Он, например, отметил частое выявление у выздоравливающих больных фагов, специфичных в отношении микроорганизмов, вызвавших заболевание и довольно быстрое по времени изменения популяций этих фагов. Всю свою жизнь он посвятил, разработке возможности применения фагов, полученных путем надлежащей селекции, как средства для лечения заболеваний, наиболее подрывавших здоровье людей в те годы. Вначале, однако, он сосредоточился на простом понимании биологии фагов. По этому первое известное сообщение об успешной фаговой терапии поступило не от д’Эрель, а от Bruynoghe и Маisin (1921), которые использовали фаг для лечения стафилококковых инфекций кожи.
Через год, будучи в институте Пастера в Сайгоне, д’Эрель оказался в тяжелом материальном положении, находясь в конфликте и имея интеллектуальные разногласия с коллективом института Пастера в Париже. Вскоре он принял предложение переехать в Нидерланды, где ему были обеспечены лучшие условия для работы по лечению инфекционных заболеваний и исследованию свойств бактериофагов. Там он опубликовал свою первую книгу и ряд статей, получил степень доктора медицинских наук .В 1925 г. он стал инспектором службы здравоохранения Лиги Наций, (Александрия, Египет), особо уполномоченным за борьбу с инфекционными заболеваниями на кораблях, проходящих по Суэцкому каналу и во время некоторых крупных мусульманских паломничеств. Фаговая терапия и санитарные мероприятия были главными средствами в его арсенале борьбы с крупными вспышками инфекционных заболеваний на Среднем Востоке и в Индии. В течение всего этого периода он продолжал публикации о своем исследовании и клинических испытаниях, оказывал помощь и давал консультации желающим изучать фаги, часто предпринимая длительные путешествия за свой счет. Одно из наиболее обширных исследований фаговой терапии, проведенное с его помощью, было Исследование Бактериофагов в 1927-1936 гг. (Summers, 1993), закончившееся тем, “что результаты, подтвержденные августейшей комиссией, кажутся убедительными” и хотя все еще остается много скептиков в отношении фаговой терапии, эти исследования заслуживают тщательного изучения.
В 1928 г. д’Эрель был приглашен в Стэнфорд, чтобы прочитать престижные лекции - Lane Lectures; его дискуссия “Бактериофаг и его клинические применения” была опубликована в виде монографии (d’ Herelle and Smith, 1930). Во время поездок по стране он прочел множество лекций в медицинских институтах и обществах. Затем он отправился в Йель, чтобы занять постоянную должность на факультете, организованную при поддержке George Smith, который перевел первые две его книги на английский язык. Он продолжал проводить летний период в Париже, работая в организованной им фаговой компании, которой руководил его зять. Компания была создана в ответ на большие потребности в высококачественных фаговых препаратах; этот период особенно хорошо описан Summers (1999). В 1933 г. д’Эрель возвратился в Европу на постоянное жительство, проводя много времени в следующие два года в Тифлисе (Тбилиси), Грузия, помогая в организации Международного Института Бактериофагов.
С самого начала, одним из главных направлений практического применения фагов была идентификация бактерий путем процесса, называемого фаготипирование – идентификации штаммов микробов с помощью определения спектра чувствительности к специфическому набору фагов. Эта методика обладает преимуществом в виду высокой специфичности многих фагов в отношении их хозяев и по-прежнему широко используется во всем мире. Высокоспецифичная способность фагов уничтожать свои бактерии-хозяева может также оказать негативный коммерческое эффект: случайное заражение фагом может быть катастрофическим для различных бродильных производств, использующих микробные технологии, таких, как производство сыра и ферментативный синтез химических веществ и вызывать финансовые бедствия
Фаговая терапия испытывалась широко, были сообщения о многочисленных успехах ее при ряде заболеваний включая дизентерию, брюшной тиф и напоминающую брюшной тиф лихорадку, холеру, пиогенные инфекции и инфекции мочевых путей. Фаги непосредственно наносили на место поражения, давали внутрь либо применяли в виде аэрозолей или клизм. Их также вводили в виде инъекций внутрикожно, в сосуды, внутримышечно, интрадуоденально, внутрибрюшинно даже внутрь легких, в сонную артерию и перикард. Сильный интерес к фаговой терапии на раннем этапе нашел отражение в том, что на эту тему опубликовано около 800 статей с 1917 по 1956 г; результаты были довольно разнообразными и подробно освещены Ackerman и Dubow (1987). Многие врачи и предприниматели очень заинтересовались возможным клиническим применением фагов и перескочили к использованию, имея как слабое представление о них самих и о микробиологии, так и дефицит базовых научных знаний вообще. Таким образом, многие из этих исследований были плохо контролируемыми или вовсе анекдотичными, многие неудачи были предсказуемыми, а в описании некоторых успехов не доставало научного смысла. Часто фаги с неизвестными свойствами, в неизвестных концентрациях давались больным без специфичного бактериологического диагноза, при этом не было никакого упоминания о катамнезе, контроле или плацебо.
На раннем этапе работы с фагами игнорировалось многое из того, что удалось понять д’Эрель часто использовались неправильные методы приготовления, “консервирования” и хранения. В одном случае д’Эрель описал испытание 20 препаратов изготовленных различными компаниями, в ходе которого выяснилось, что ни один из них не содержал активные бактериофаги (Summers, 1999).
В другом случае препарат рекламировался как содержащий ряд различных фагов, но, как оказалось, ответственный технолог решил, что легче выращивать их в виде одной большой партии, чем отдельно. Неудивительно, что проверка продукта выявила подавление одним фагом всех остальных, и препарат фактически не был поливалентным. Так был получен фаг Т7, РНК-полимераза которого сейчас играет большую роль в биотехнологии (личное сообщение William Summers). В целом, исключая несколько исследовательских центров, контроль качества не производился. Крупные клинические исследования были редкостью, и результаты этих немногих работ были большей частью недоступны за пределами Восточной Европы.
В 1931 г. Советом по Фармации и Химии Американской Медицинской Ассоциации был подготовлен обширный обзор по фаговой терапии (Eaton and Bayne-Jones, 1931). Его целью было: “(а) представить резюме и обсуждения (1) экспериментально установленных фактов, связанных с феноменом бактериофагов, (2) лабораторных и клинических данных "за" и "против" терапевтической применимости бактериофагов и (3) выявить имеет ли отношение так называемый антивирус к материалам, содержащим бактериофаги и (б) служить основой для изучения свойств некоторых коммерческих препаратов”. Этот отчет, имевший 150 ссылок, был крупнейшей попыткой обзора, по крайней мере, тех статей и обзоров, которые рассматривались как наиболее значимые. Оценивая этот отчет, важно понять, насколько мало было известно тогда о бактериофагах. Фактически первым заключением было: “Экспериментальные исследования литического агента, названного “бактериофагом”, не раскрыли его природы. Теория д’Эрель о том, что этот материал является живым вирусом, паразитирующим в бактериях, не доказана. Напротив, факты указывают на то, что этот материал неживой, возможно является ферментом”. В ретроспективе доказательство того, что фаги являются вирусами, выглядит веско, и трудно понять‚ как можно было придти к такому заключению, явно повлиявшему на все остальные. Они включали в себя следующее:
1) Поскольку окончательно не показано, что бактериофаг является живым организмом, не обосновано объяснять его действия на культуры бактерий или его возможное терапевтическое действие свойствами живого вещества. 2) В то время как в (бактериальной) культуре бактериофаг растворяет чувствительные бактерии и вызывает многочисленные модификации микроорганизмов, его литическое действие в организме ингибируется или сильно затрудняется кровью и другими жидкостями тела. 3) Материал, называемый бактериофагом, обычно является фильтратом лизированных микроорганизмов, содержащим, в дополнение к литическому началу, антигенные бактериальные вещества, продукты бактериального роста и составляющие культуральной среды. Эффект всех этих компонентов необходимо принимать во внимание всякий раз, когда испытывается терапевтическое действие. 4) Обзор литературы об использовании бактериофагов в лечении инфекций выявил, что обоснование терапевтической значимости литических фильтратов является большей частью спорным. Только при лечении местных стрептококковых инфекций и, возможно, цистита, представлены вполне убедительные данные”.
Эта оценка явно оказала сильное влияние на инвестирование серьезных исследований фаговой терапии медицинской общественностью, по крайней мере, в Соединенных Штатах. Поднятые вопросы, по-прежнему требуют рассмотрения, как, в отношений многих описанных здесь исследований на животных или на людей, которые, казалось, были малоуспешными или безуспешными, так и в отношении таких возможно неправильных объяснений успехов, как сильная стимуляция естественных иммунных механизмов продуктами распада бактерий, содержащимися в используемых лизатах. Далее в 40-х гг. стали широкодоступны новые “чудесные” антибиотики, такие как пенициллин, и Западный мир большей частью отказался от фаговой терапии.
Специфическе проблемы ранних работ по фаговой терапии
Сегодня многие полагают, что в первой половине этого века была показана неэффективность фаговой терапии. Однако получилось так, что она просто не исследована в полной мере и должным образом, так что иная ее оценка вполне оправдана. По этому важно рассмотреть во всех деталях как возможные причины проблем раннего периода, так и вопросы касающиеся эффективности, а именно:
1) Недостаточность понимания гетерогенности и экологии как фагов, так и вовлеченных бактерий.
2) Неудача в селекции фагов, высоко вирулентных против бактерий-мишеней, до их использования у больных.
3) Использование моно фагов при инфекциях, вызываемых несколькими различными бактериями.
4) Появление резистентных штаммов бактерий. Они могут возникнуть путем селекции резистентных мутантов (это часто происходит, при использовании только одного штамма фага против конкретной бактерии) или путем лизогенизации (если используются умеренные фаги, как обсуждается ниже).
5) Неправильная классификация фагов или ошибки в отношении титра препаратов, некоторые из которых были полностью неактивны.
6) Неудача в нейтрализации низких значений желудочного рН при использовании пероральных препаратов.
7) Инактивация бактериофагов специфическими и неспецифическими факторами в жидкостях организма.
8) Высвобождение эндотоксинов вследствие массивного лизиса бактерий внутри организма (что именуется врачами реакцией Herxheimer). Это может привести к токсическому шоку и является потенциальной проблемой также и для химических антибиотиков.
9) Недостаточная готовность и надежность бактериологических лабораторий для тщательной идентификации причинных патогенов, необходимой ввиду специфичности фаговой терапии.
Природа фагов
Несмотря на то, что явление бактериофагии интенсивно изучается более пятидесяти лет, на природу фагов нет единой точки зрения, и этот вопрос до сих пор остается спорным. В нашей стране и за рубежом в специальной печати и на конференциях неоднократно возникали горячие дискуссии на эту тему. И это не случайно. Вопрос о происхождении фагов, как и других вирусов, имеет большое значение, так как с ним тесно связано решение многих актуальнейших задач современной биологии: происхождение жизни, возможные формы существования живого; существование живых существ, не имеющих клеточной структуры; происхождение клеточных форм жизни; развитие, изменчивость и видообразование у микроорганизмов и др.
До настоящего времени все еще существуют диаметрально противоположные точки зрения на природу вирусов, в том числе и фагов. По мнению одних ученых, фаги относятся к живым организмам; другие рассматривают их как особые вещества типа ферментов.
Важно отметить, что те исследователи, которые относят фаги к живым организмам, различно трактуют вопрос об их происхождении. Одни исследователи считают, что фаги, как и вирусы человека, животных и растений, произошли от древнейших доклеточных форм, которые в процессе эволюции приспособились к паразитированию в первичных одноклеточных организмах и в дальнейшем эволюционировали вместе со своими хозяевами. Таким путем, как думают эти ученые, возникли фаги микроорганизмов, которые по своему отношению к клетке-хозяину являются паразитами экзогенного, т.е. внешнего, происхождения. Другие же считают, что происхождение фагов связано тем или иным образом с клеткой своего теперешнего хозяина (эндогенное происхождение).
По мнению ученых, рассматривающих фаг как фермент эндогенного происхождения, фаговая частица является продуктом жизнедеятельности микробной клетки. При попадании в клетку фаги вызывают каталитически протекающие процессы образования активного фага, способного разрушать микробную клетку. А размножение фага в клетке происходит приблизительно так же, как образование активного фермента из его неактивного предшественника — профермента.
Какая же из изложенных точек зрения на природу фага является наиболее приемлемой, исходя из современных знаний о свойствах фага и его взаимоотношений с клеткой-хозяином? Является ли фаг живым существом или это — вещество подобное ферменту? За последние годы благодаря применению новейших современных методов исследования (электронная микроскопия, меченые атомы) знания о структуре фагов, их химическом составе, особенностях размножения значительно расширились. Фаговая частица оказалась довольно сложно организованной. Она содержит основные химические соединения, свойственные живому организму,— нуклеиновые кислоты и белок. Подобно другим живым существам, фаги способны изменять все свои свойства. Поэтому рассматривать их как ферменты нет никаких оснований. Верно, они не обладают собственным обменом веществ. Они являются абсолютными паразитами, живущими полностью за счет клетки-хозяина.
Следовательно, фаги логично рассматривать как особые формы живых существ. Однако вопрос о происхождении фагов пока еще нельзя считать окончательно решенным.
Распространение фагов
В настоящее время найдены, фаги, лизирующие клетки микроорганизмов, принадлежащих ко всем систематическим группам, как патогенных для человека, животных и растений, так и сапрофитных (непатогенных).
До недавнего времени не было ясно, существуют ли фаги против плесневых грибов и дрожжей. В последние годы найдены фаги, активные против грибов родов пенициллов, аспергил-лов и других, а также против некоторых дрожжей. Интересно отметить, что вирус удалось выявить и у тех видов пенициллов, которые применяются в промышленности для получения пенициллина. Не выявлены вирусы, активные против простейших животных, а также истинных спирохет.
В природных условиях фаги встречаются в тех местах, где есть чувствительные к ним бактерии. Чем богаче тот или иной субстрат (почва, вода, выделения человека и животных и т. д.) микроорганизмами, тем в большем количестве в нем встречаются соответствующие фаги. Так, фаги, лизирующие клетки всех видов почвенных микроорганизмов, находятся в почвах. Особенно богаты фагами черноземы и почвы, в которые вносились органические удобрения. Фаги, активные против разных видов кишечной, дизентерийной, тифозной и паратифозной палочек, часто встречаются в содержимом кишечника человека и животных, сточных водах и загрязненных водоемах. Фаги фитопатогенных микроорганизмов успешнее всего выделяются из остатков растений, пораженных этими микробами
Итак, те субстраты, на которых развиваются определенные формы микроорганизмов, также благоприятны для существования соответствующих фагов.
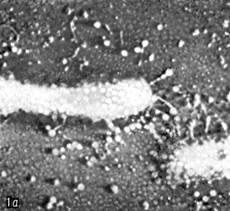
Иллюстрация 1: Escherichia coli атакуемая фагами
Морфология фагов
Применение современных электронных микроскопов, а также усовершенствование методов приготовления препаратов для электронной микроскопии позволили более детально изучить тонкую структуру фагов. Оказалось, что она весьма разнообразна и у многих фагов более сложна, чем структура вирусов растений и ряда вирусов человека и животных.
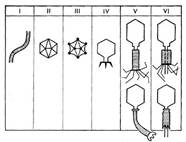
Иллюстрация 2: Морфологические типы фагов
Разные фаги отличаются друг от друга не только по форме, величине и сложности своей организации, но и по химическому составу. Оказалось, что фаги, лизирующие микроорганизмы различных групп, могут быть вполне идентичными по своей морфологии. В то же время фаги, активные против одной и той же культуры, могут резко различаться по своей структуре. Так, например, среди фагов, способных лизировать разные штаммы кишечной палочки, выявлены все известные морфологические типы фагов.
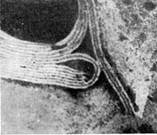
Иллюстрация 3: Палочковидные, или нитевидные, фаги. Увел. X 400 000.
Частицы (или вирионы) большинства известных фагов имеют форму сперматозоида. Они состоят из головки (или капсида) и отростка. Наряду с этим есть фаги, которые состоят из одной головки, без отростка, и фаги, имеющие форму палочки (палочковидные или нитевидные фаги).
По форме частиц фаги делятся на шесть основных морфологических типов (групп): (рис.2) палочковидные или нитевидные фаги; фаги, состоящие из одной головки, без отростка; фаги, состоящие из головки, на которой имеется несколько небольших выступов; фаги, состоящие из головки и весьма короткого отростка; фаги, имеющие головку и длинный отросток, чехол которого не может сокращаться; фаги, имеющие головку и длинный отросток, чехол которого может сокращаться.
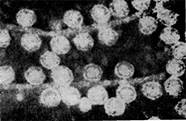
Иллюстрация 4: Фаги 2 морфологического типа, частица состоит из одной головки. Увел. X 600 000
Размеры фагов принято обозначать в милли-микрометрах (1 миллимикрометр — миллионная часть миллиметра) или в ангстремах (10 А = 1 миллимикрометр).
Фаги первого морфологического типа — палочковидные или нитевидные — выявлены у кишечной, синегнойной, чудесной палочек и других бактерий. Средние размеры их: длина — от 7000 до 8500 А, ширина — от 50 до 80 А (рис. 3). Эти фаги отличаются от всех остальных не только большой специфичностью, но и рядом других важных свойств.
Фаги второго морфологического типа. Частица их состоит из одной головки гексагональной (шестигранной) формы на плоскости. Частицы очень мелкие, средний размер их 230—300 А в диаметре (рис. 4).
У фагов третьего морфологического типа форма и размеры головки такие же, как у фагов второго типа, но у их головок имеются обычно несколько очень коротких выступов (рис. 5). Возможно, эти выступы являются аналогами отростков.
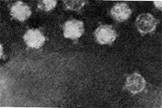
Иллюстрация 5: Фаги третьего морфологического типа от головки отходят небольшие выступы
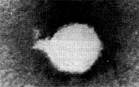
Иллюстрация 6: Фаг 4 морф. типа. Частица состоит из головки и короткого отростка Увел. х500 000
Фаги 2-го и 3-го морфологических типов отличаются постоянством формы и размеров, независимо от того, против каких микроорганизмов они активны. Эти фаги относятся к мелким формам.
Фаги 4-го морфологического типа. Частица состоит из головки, размеры которой варьирую от 400 до 640 А в диаметре, и очень короткого отростка (рис. 6).Длина и ширина отростка от 70 до 200 А.
Фаги пятого морфологического типа наиболее широко распространены. Головка у частиц гексагональной, формы различных размеров — от 500 до 4250 А в диаметре. Размеры отростка: длина — от 1700 до 5000 А, ширина — от 70 до 120 А (рис. 7). Чехол отростка не способен сокращаться.
Фаги шестого морфологического типа также широко распространены. Головка частицы различной формы и размеров — от 600 до 1500 А в диаметре, гексагональная. Размеры отростка: длина — от 800 до 2890 А, ширина — от 140 до 370 А. Важной особенностью фагов этой группы является то, что чехол, окружающий отросток, способен сокращаться, в результате чего становится видимым внутренний стержень отростка (рис.8).
Головки всех фагов состоят из внутреннего содержимого — нуклеиновой кислоты - и окружены белковой оболочкой. Отросток фагов весьма сложен. Он обычно состоит из следующих структур: наружного чехла (или оболочки), внутреннего стержня с канальцем, базальной пластинки, оканчивающейся выступами (типа шипов) и нитевидными структурами. Чехол отростка состоит из субъединиц белковой природы, собранных в спираль. В результате этого он приобретает вид гофрированной трубки. В верхней части отростка многих фагов имеется образование, которое называется воротничком. На рисунке 9 схематически изображена тонкая структура фаговой частицы.
Химический состав фагов
Изучение химического состава фагов стало возможно лишь тогда, когда были усовершенствованы методы получения в больших количествах очищенных препаратов фага. В настоящее время изучен химический состав фагов, принадлежащих к разным морфологическим типам и поражающих микроорганизмы почти всех систематических групп.
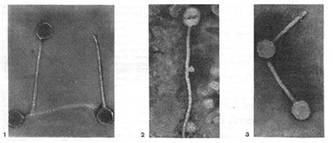
Иллюстрация 7: Разные фаги пятого морфологического типа, частица состоит из головки и длинного отростка, чехол которого не способен сокращаться. 1,2- увел. X 225 000, 3 - увел. X250 000
Основными компонентами фагов являются белки и нуклеиновые кислоты. Важно отметить, что фаги, как и другие вирусы, содержат только один тип нуклеиновой кислоты — дезоксирибонуклеиновую (ДНК) или рибонуклеиновую (РНК). Этим свойством вирусы отличаются от микроорганизмов, содержащих в клетках оба типа нуклеиновых кислот.
Нуклеиновая кислота находится в головке. Внутри головки фагов обнаружено также небольшое количество белка (около 3%).
Таким образом, по химическому составу фаги являются нуклеопротеидами. В зависимости от типа своей нуклеиновой кислоты фаги делятся на ДНК-овые и РНК-овые. Количество белка и нуклеиновой кислоты у разных фагов разное. У некоторых фагов содержание их почти одинаковое и каждый из этих компонентов составляет около 50%. У других фагов соотношение между этими основными компонентами может быть различно.

Иллюстрация 8: Фаг шестого морфологического типа, частица состоит из головки и длинного отростка, чехол которого способен к сокращению. Увел, около 400 000.
Кроме указанных основных компонентов, фаги содержат в небольших количествах углеводы и некоторые преимущественно нейтральные жиры.
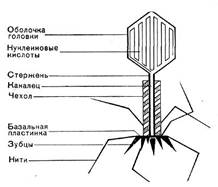
Иллюстрация 9: Схема строения фаговой частицы.
Все известные фаги второго морфологического типа РНК-овые. Среди фагов третьего морфологического типа встречаются как РНК-овые, так и ДНК-овые формы. Фаги остальных морфологических типов — ДНК-овые.
Антигенные свойства фагов
Известно, что при введении в организм животного подкожно или внутривенно белка, бактериальных клеток, некоторых продуктов жизнедеятельности микроорганизмов и других веществ в крови животного вырабатываются вещества, названные антителами. Вещества, способные вызывать образование антител, называются антигенами.
Антитела очень специфичны и способны вступать в реакции только с теми антигенами, которые вызвали их образование. Они или связывают соответствующие антигены, или нейтрализуют их, или осаждают, или растворяют.
Оказалось, что все фаги обладают антигенными свойствами. При введении фага в организм животного в сыворотке крови образуются специфические антитела, способные действовать только против данного фага. Такие сыворотки называются антифаговыми. Когда фаг смешивается со специфической антифаговой сывороткой, происходит инактивация фага — фаг теряет способность вызывать лизис чувствительных к нему микробов.
Так как каждая антифаговая сыворотка специфична, ее можно успешно применять для идентификации и классификации фагов и очистки микробной культуры от фага. При помощи сыворотки удалось доказать, что белок оболочки фага отличается от белка оболочки отростка и от белка базальной пластинки и ее нитевидных образований, что говорит о сложности структуры фаговой частицы. По антигенным свойствам фаг резко отличается от чувствительных к нему микробов.
Механизм воздействия бактериофагов на бактериальную клетку
Размножение фагов
Взаимоотношения между фагом и чувствительной к нему клеткой очень сложны и не всегда завершаются лизисом клетки и размножением в ней фага. Одни бактериофаги весьма специфичны и способны лизировать клетки только одного какого-либо вида микроорганизмов (монофаги), другие — клетки разных видов (полифаги). Рассмотрим такую инфекцию клетки, которая заканчивается гибелью клетки и размножением в ней фага. Такая инфекция называется продуктивной.
Важнейшей особенностью размножения фага является то, что оно может происходить только в живых клетках, находящихся в стадии роста.
В мертвых клетках, а также продуктах клеточного обмена размножение фага не происходит.. По характеру взаимодействия с микробной клеткой различают вирулентные и умеренные Б. Процесс взаимодействия вирулентного Б. с клеткой весьма сложный и состоит из следующих последовательно протекающих этапов (рис. 10): 1) адсорбция фаговой частицы на поверхности микробной клетки; 2) проникновение содержимого головки фаговой частицы (нуклеиновой кислоты) в микробную клетку; 3) внутриклеточное развитие фага, заканчивающееся образованием новых фаговых частиц; 4) лизис клетки и выход из нее новых фагов.
Время с момента инфицирования клетки фагом до лизиса клетки называется латентным или скрытым периодом. Продолжительность этого периода различна для разных типов фага, зависит от окружающей температуры, состава среды и других факторов. Латентный период фагов, специфичных для одних бактерий, 15—40 мин, для других — 5 ч и более. У фагов актиномицетов латентный период может быть еще продолжительнее. При низкой температуре латентный период значительно увеличивается.
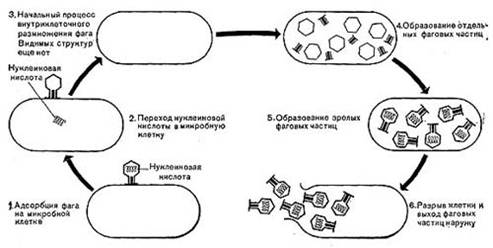
Иллюстрация 10: Схема размножения фага.
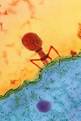
Иллюстрация 11: Адсорбция фага на клетке
Из всех этапов размножения фага наиболее изучен первый — адсорбция.
Адсорбция фага на клетке — реакция весьма специфичная. В клеточной стенке бактерий имеются особые структуры (рецепторы), к которым могут прикрепиться фаги. Адсорбируются на рецепторах только те фаги, к которым чувствительна клетка.
Фаги, имеющие отростки, прикрепляются к микробной стенке свободным концом отростка. Нитевидные фаги, а также фаги, не имеющие отростков, адсорбируются не на микробной стенке, а на нитевидных структурах, окружающих стенку, — фимбриях. Описаны фаги, которые прикрепляются отростком к бактериальным жгутикам. У некоторых фагов процесс адсорбции может осуществляться лишь в том случае, когда в среде имеются определенные вещества — кофакторы: аминокислоты (триптофан, тирозин и др.) или соли (кальциевые, магниевые).
На конце фагового отростка имеется особый фермент типа лизоцима. После адсорбции фага под влиянием этого фермента происходит растворение стенки микробной клетки и содержимое головки фага — нуклеиновая кислота — перекачивается в микробную клетку. Этим завершается второй этап процесса размножения фага.
Остальные структуры фаговой частицы — оболочка головки, отросток и его субструктуры — внутрь инфицированной фагом клетки не попадают. Их роль заключается в обеспечении сохранности фаговой частицы, находящейся вне клетки, и содействии проникновению фаговой нуклеиновой кислоты в клетку при инфекции.
Иллюстрация 12: Мелкие (едва видимые) негативные колонии актинофага. Увел. 6:10
У нитевидных фагов, в отличие от других видов фагов, внутрь клетки проникает весь белок или его часть. После проникновения нуклеиновой кислоты фага в клетку начинается сложный процесс внутриклеточного размножения фага. Под влиянием нуклеиновой кислоты фага резко изменяется весь обмен микробной клетки. Основные процессы, протекающие в инфицированной клетке, направлены на образование новых фаговых частиц. Инъецированная ДНК подавляет синтезирующие механизмы клетки, заставляя ее синтезировать ДНК и белки бактериофага. Из образовавшихся в разных частях клетки в разное время фаговой нуклеиновой кислоты и белка формируются новые фаговые частицы (сборка Б.). Вначале формируются отдельно головки и отростки, которые затем объединяются в зрелые фаговые частицы. К этому времени внутри клетки образуется особый литический фермент, который вызывает лизис клетки изнутри. Клетка распадается, и новые зрелые частицы фага выходят наружу.
Иллюстрация 13: Мелкие негативные колонии актинофага Увел. 8 : 9.
Количество новых фаговых частиц, образуемых одной клеткой при фаговой инфекции, называют выходом фага или его урожайностью. Выход фага зависит от свойств данного фага и не зависит от клетки-хозяина и ее размеров. Одни фаги отличаются очень низким выходом (5—50 частиц на клетку), у других выход значительно выше (от 1000 до 2500). Особенно высоким выходом отличаются мелкие РНК-овые фаги (свыше 20 000 частиц на клетку). Если большое количество бактериальных клеток смешать с