Энтальпия образования индивидуальных веществ. Прогнозирование энтальпии образования методом Бенсона
o Энтальпия образования
o Прогнозирование энтальпии образования
o Прогнозирование органических соединений методом Бенсона по атомам с их первым окружением
o Некоторые многовалентные группы метода Бенсона для идеально-газового состояния
o Алканы
o Групповые составляющие для расчета идеально-газовых свойств по Бенсону
o Циклоалканы
o Алкены
o Ацетиленовые углеводороды
o Ароматические углеводороды
o Кислородсодержащие соединения
Наилучшее решение вопросов разработки процессов химической технологии и аппаратуры для их проведения возможно лишь при наличии надежной информации по физико-химическим и термодинамическим свойствам химических соединений. Подобная информация часто составляет от 50 до 90% исходных данных при проектировании.
Для практики предпочтительными являются экспериментальные данные. На протяжении многих лет собрано и обработано огромное количество таких данных. Эти сведения имеются в многочисленных компиляциях и справочниках. В некоторых из них приводятся все известные в настоящее время значения термодинамических и физико-химических характеристик и дается их критический анализ. В других содержатся только рекомендованные авторами величины, часто являющиеся либо средними значениями, либо результатом статистической обработки всего массива накопленных сведений. Однако быстрый прогресс технологии и вовлечение в сферу деятельности все большего количества новых веществ и материалов обусловливают значительный разрыв между потребностью в данных и их наличием. Определение же экспериментальных величин в широких параметрах состояния и составов часто бывает затруднительным, а иногда и просто невозможным.
По этой причине инженер зачастую вынужден полагаться на разнообразные методы расчета и прогнозирования свойств веществ. Следует иметь в виду, что термины “расчет” и “прогноз” час то используются как синонимы, хотя второй из них несет в себе честное признание того факта, что результат может быть правильным только отчасти. Расчеты же могут основываться на теории, на корреляции экспериментальных значений или на комбинации того и другого.
Энтальпия образования (enthalpy of formation) является основным свойством, используемым при решении многих теоретических и практических задач. Знание энтальпий образования реагентов позволяет вычислить тепловые эффекты интересующих реакций, что необходимо при оценке адиабатического перепада температур в зоне реакции, формировании требований к конструкции реактора и технологическим особенностям химического процесса. Энтальпии образования веществ необходимы при выполнении количественного термодинамического анализа процессов, определении теоретической степени конверсии реагентов, выборе условий проведения химического превращения и т.п. Качество выполненного термодинамического анализа во многом зависит от надежности сведений по энтальпиям образования веществ.
Единицами измерения энтальпии являются кДж/моль и Дж/моль. В справочной литературе прежних лет энтальпии образования часто представлены в ккал/моль (1 кал = 4,184 Дж, 1 ккал = 4,184 кДж).
Энтальпия образования (![]() ) соединения в узком смысле есть стандартное изменение энтальпии в реакции образования данного вещества из элементов или простых веществ. Простыми веществами являются химические элементы, находящиеся при рассматриваемой температуре в их естественном фазовом и химическом состояниях.
) соединения в узком смысле есть стандартное изменение энтальпии в реакции образования данного вещества из элементов или простых веществ. Простыми веществами являются химические элементы, находящиеся при рассматриваемой температуре в их естественном фазовом и химическом состояниях.
В качестве стандартного состояния вещества выбирается такое его состояние, при котором это вещество устойчиво при стандартном давлении, равном 1 атм (101325 Па). Конденсированное состояние вещества является стандартным вплоть до тех температур, при которых давление его насыщенного пара достигает 1 атм. Выше этих температур в качестве стандартного выбирается состояние идеального газа.
Для простых веществ, участвующих в формировании молекул большинства органических соединений, стандартным состоянием при 298,15 К является:
· для углерода - графит;
· для водорода, кислорода, азота, фтора и хлора - идеальный двухатомный газ;
· для брома - двухатомная жидкость;
· для иода и серы - кристаллическое состояние, двухатомное и одноатомное соответственно.
Абсолютные значения энтальпий не могут быть определены, поскольку они включают абсолютные значения внутренней энергии. Необходимость определения энтальпий образования соединений потребовала достижения международного соглашения, по которому были приняты равными нулю значения ![]() элементов и простых веществ, находящихся в стандартном состоянии.
элементов и простых веществ, находящихся в стандартном состоянии.
Величина и знак ![]() веществ со сложным строением молекул могут быть различными. Объясняется это следующим. Образование вещества из свободных атомов всегда сопровождается выделением энергии,
веществ со сложным строением молекул могут быть различными. Объясняется это следующим. Образование вещества из свободных атомов всегда сопровождается выделением энергии, ![]() полученных при этом веществ отрицательна. Однако при образовании вещества из простых веществ, состоящих из двухатомных молекул (H2, О2, N2, Cl2 и пр.) или находящихся в конденсированном состоянии (углерод, бром и т.п.), некоторое количество энергии требуется для разрыва связей в молекулах этих простых веществ или для перевода их в газообразное состояние. В результате этого энтальпия образования может быть и положительной, и отрицательной, и равной нулю величиной.
полученных при этом веществ отрицательна. Однако при образовании вещества из простых веществ, состоящих из двухатомных молекул (H2, О2, N2, Cl2 и пр.) или находящихся в конденсированном состоянии (углерод, бром и т.п.), некоторое количество энергии требуется для разрыва связей в молекулах этих простых веществ или для перевода их в газообразное состояние. В результате этого энтальпия образования может быть и положительной, и отрицательной, и равной нулю величиной.
В общем случае значение и знак ![]() не дают оснований для каких-либо утверждений относительно термодинамической стабильности вещества, так как она зависит не только от энтальпийной, но и от энтропийной составляющей изменения свободной энергии при образовании этого вещества. Тем не менее, для сопоставления термодинамической стабильности представителей одной гомологической группы или соединений с близким строением молекул может быть достаточно информативным, в первом приближении, анализ их энтальпий образования. В этом случае вещество, имеющее меньшее значение энтальпии образования, обладает большей термодинамической стабильностью.
не дают оснований для каких-либо утверждений относительно термодинамической стабильности вещества, так как она зависит не только от энтальпийной, но и от энтропийной составляющей изменения свободной энергии при образовании этого вещества. Тем не менее, для сопоставления термодинамической стабильности представителей одной гомологической группы или соединений с близким строением молекул может быть достаточно информативным, в первом приближении, анализ их энтальпий образования. В этом случае вещество, имеющее меньшее значение энтальпии образования, обладает большей термодинамической стабильностью.
Для большинства соединений реакции их образования из простых веществ не могут быть осуществлены на практике. Основным источником фактической информации об энтальпиях образования органических соединений являются экспериментальные данные по энтальпиям их сгорания (![]() ), полученные калориметрическим методом. Накопленные к настоящему времени и рекомендуемые значения
), полученные калориметрическим методом. Накопленные к настоящему времени и рекомендуемые значения ![]() и
и ![]() содержатся в компиляциях (1-4). До настоящего времени справочные сведения об
содержатся в компиляциях (1-4). До настоящего времени справочные сведения об ![]() были представлены исключительно калориметрическими данными. Современные эмпирические методы прогнозирования
были представлены исключительно калориметрическими данными. Современные эмпирические методы прогнозирования ![]() также базируются только на калориметрических данных. При этом следует отметить, что информация, уникальная по спектру задействованных веществ, объему выполненных исследований и точности полученных термодинамических характеристик, содержится в результатах изучения химического равновесия. На наш взгляд, эффективное использование этих сведений позволит существенно расширить прогностические возможности методов массовых расчетов
также базируются только на калориметрических данных. При этом следует отметить, что информация, уникальная по спектру задействованных веществ, объему выполненных исследований и точности полученных термодинамических характеристик, содержится в результатах изучения химического равновесия. На наш взгляд, эффективное использование этих сведений позволит существенно расширить прогностические возможности методов массовых расчетов ![]() органических веществ.
органических веществ.
ПРОГНОЗИРОВАНИЕ ЭнтальпиЙ образования (1-8)
Основные методы прогнозирования энтальпий образования органических соединений относятся к ![]() , то есть характеризуют свойство вещества, находящегося в состоянии идеального газа при давлении 1 атм. и температуре 298,15 К, которую часто называют стандартной. Среди методов массовых расчетов
, то есть характеризуют свойство вещества, находящегося в состоянии идеального газа при давлении 1 атм. и температуре 298,15 К, которую часто называют стандартной. Среди методов массовых расчетов ![]() особого внимания заслуживают методы молекулярной механики и аддитивные методы (лат. additio - прибавление). Большинство полуэмпирических методов не обеспечивает требуемого качества прогноза. Неэмпирические методы не дают прямого выхода на энтальпии образования веществ и к тому же до сих пор являются малодоступными для расчета свойств органических веществ со сложным строением молекул.
особого внимания заслуживают методы молекулярной механики и аддитивные методы (лат. additio - прибавление). Большинство полуэмпирических методов не обеспечивает требуемого качества прогноза. Неэмпирические методы не дают прямого выхода на энтальпии образования веществ и к тому же до сих пор являются малодоступными для расчета свойств органических веществ со сложным строением молекул.
В группе методов молекулярной механики нами накоплен значительный опыт по использованию метода ММХ (на базе силового поля Эллинджера). Метод хорошо зарекомендовал себя в приложении к ![]() алканов. Однако уже для ароматических соединений его целесообразно использовать не для расчета энтальпий образования, а для оценки эффектов взаимодействия заместителей в молекуле, т.е. для разностей энтальпий образования изомеров. Для большинства галогенорганических, кислород-, азот- и серосодержащих соединений метод дает смещенные оценки
алканов. Однако уже для ароматических соединений его целесообразно использовать не для расчета энтальпий образования, а для оценки эффектов взаимодействия заместителей в молекуле, т.е. для разностей энтальпий образования изомеров. Для большинства галогенорганических, кислород-, азот- и серосодержащих соединений метод дает смещенные оценки ![]() . Тем не менее, этот метод следует применять во всех случаях для экспрессной оценки свойства. Как и любой другой метод, он требует подкрепления результатов сведениями, полученными другим методом прогнозирования. Метод молекулярной механики имеет прекрасный интерфейс и исключительно результативен как источник информации о строении молекул и их геометрических параметрах.
. Тем не менее, этот метод следует применять во всех случаях для экспрессной оценки свойства. Как и любой другой метод, он требует подкрепления результатов сведениями, полученными другим методом прогнозирования. Метод молекулярной механики имеет прекрасный интерфейс и исключительно результативен как источник информации о строении молекул и их геометрических параметрах.
При отсутствии справочных данных для прогнозирования ![]() в настоящее время широко используются различные аддитивные методы. С момента создания основных аддитивных методов прогнозирования свойств органических веществ, находящихся в состоянии идеального газа, прошел значительный период времени, однако они сохраняют свою значимость, несмотря на становящиеся все более доступными методы молекулярного моделирования. Эти методы эффективны в тех случаях, когда свойство изменяется линейно при изменении количества однотипных фрагментов в молекуле. Строго аддитивной является, например, молекулярная масса вещества. Для энтальпий образования органических соединений аддитивный подход является во многих случаях лишь некоторым приближением в расчете. Дело в том, что даже в гомологической группе
в настоящее время широко используются различные аддитивные методы. С момента создания основных аддитивных методов прогнозирования свойств органических веществ, находящихся в состоянии идеального газа, прошел значительный период времени, однако они сохраняют свою значимость, несмотря на становящиеся все более доступными методы молекулярного моделирования. Эти методы эффективны в тех случаях, когда свойство изменяется линейно при изменении количества однотипных фрагментов в молекуле. Строго аддитивной является, например, молекулярная масса вещества. Для энтальпий образования органических соединений аддитивный подход является во многих случаях лишь некоторым приближением в расчете. Дело в том, что даже в гомологической группе ![]() изменяется нелинейно с изменением числа углеродных атомов в молекуле (рис. 1.1).
изменяется нелинейно с изменением числа углеродных атомов в молекуле (рис. 1.1).
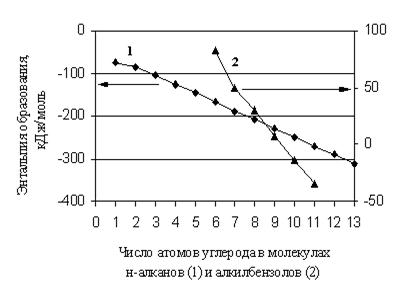
Рис. 1.1. Зависимость энтальпии образования н-алканов и алкил бензолов от числа атомов углерода в их молекулах
Таким образом, гомологическая разность не является величиной постоянной, особенно для первых членов гомологических групп. Точно так же при увеличении количества заместителей одного вида в молекулах органических веществ очень часто приходится говорить об отклонении от аддитивности в ![]() . Однако при введении поправок на неаддитивность методы данной группы работают вполне удовлетворительно, если степень и глубина их детализации достаточны и отвечают точности современного эксперимента.
. Однако при введении поправок на неаддитивность методы данной группы работают вполне удовлетворительно, если степень и глубина их детализации достаточны и отвечают точности современного эксперимента.
В зависимости от принятой идеологии в качестве носителя структурной и количественной информации в аддитивных методах могут выступать составляющие молекулу атомы, группы атомов или связи. Большинство методов прогнозирования построено таким образом, что по мере расширения базы данных по энтальпиям образования относительно легко могут быть уточнены значения парциальных вкладов или введены новые поправки.
Общий подход к прогнозированию энтальпий образования веществ предполагает вычисление ![]() с последующим, при необходимости, переходом к идеально-газовым энтальпиям образования при других температурах или к
с последующим, при необходимости, переходом к идеально-газовым энтальпиям образования при других температурах или к ![]() , т.е. к свойству вещества в реальном состоянии.
, т.е. к свойству вещества в реальном состоянии.
Из всего разнообразия аддитивных методов расчета ![]() нами рассматриваются два; групповой метод Бенсона по атомам с их первым окружением и метод Татевского по связям.
нами рассматриваются два; групповой метод Бенсона по атомам с их первым окружением и метод Татевского по связям.
Прогнозирование ![]() органических соединений методом Бенсона по атомам с их первым окружением
органических соединений методом Бенсона по атомам с их первым окружением
Следует признать, что из всего многообразия аддитивных схем для прогнозирования энтальпий образования органических веществ метод Бенсона в течение продолжительного периода применяется наиболее широко. Объясняется это, вероятно, тем, что этим методом охвачен наиболее широкий круг соединений. Для оперативной оценки ![]() абсолютного большинства соединений без привлечения каких-либо технических средств метод, пожалуй, не имеет себе равных. Совершенно очевидно, что ценой его универсальности является точность прогноза. Поэтому при использовании метода необходимо знать о неизбежных его ограничениях. На основные из них, являющиеся результатом нашей широкой апробации метода, мы постараемся обратить внимание потенциальных пользователей.
абсолютного большинства соединений без привлечения каких-либо технических средств метод, пожалуй, не имеет себе равных. Совершенно очевидно, что ценой его универсальности является точность прогноза. Поэтому при использовании метода необходимо знать о неизбежных его ограничениях. На основные из них, являющиеся результатом нашей широкой апробации метода, мы постараемся обратить внимание потенциальных пользователей.
Метод Бенсона принято называть групповым, хотя в качестве структурной единицы в нем избран атомс его первым окружением. Метод разработан автором для расчета следующих идеально-газовых свойств веществ: теплоемкости ![]() при температурах, кратных 100 градусам, энтальпии образования
при температурах, кратных 100 градусам, энтальпии образования![]() и энтропии
и энтропии ![]() .
.
По мере развития метода автор несколько изменял символику групп. Однако при некотором навыке работы с методом это не создает каких-либо ощутимых трудностей. Нами используется последняя редакция метода (5).
В табл. 1.1. приведены некоторые из наиболее распространенных групп для элементов C, N, O и S. В колонке “валентность” показано число одновалентных групп, таких как атом водорода или галогена, которые могут быть связаны с рассматриваемой группой.
Значения парциальных вкладов в свойства и специфические поправки приведены в табл. 1.2. Мы сочли себя вправе сделать некоторые дополнения к авторской редакции таблицы. Эти дополнения касаются только поправок, учитывающих взаимодействие соседних заместителей в молекулах алкилароматических соединений и галогеналкилбензолов. Они получены на основе экспериментальных данных или вычислены методом молекулярной механики ММХ.
Таблица достаточно объемна. Знакомство с ее структурой и приемы работы с методом изложены ниже в приложении к соединениям различных классов и сопровождены конкретными примерами.
Таблица 1.1
Некоторые многовалентные группы метода Бенсонадля идеально-газового состояния
| Группа | Валентность | Комментарий |
С | 4 | Четырехвалентный углерод в молекулах алканов, циклоалканов и в алкильных или циклоалкильных заместителях |
=С | 2 | Углерод при двойной связи в молекулах алкенов, циклоалкенов и в алкенильных или циклоалкенильных заместителях; обращаем внимание на то, что символ Cd не относится к атому углерода при двойной связи, а принадлежит кадмию |
С | 1 | Углерод ароматического ядра, не принадлежащий узловым атомам углерода в соединениях с конденсированными ядрами |
С | 3 | Узловой углеродный атом ароматических углеводородов с конденсированными ядрами |
Ct | 1 | Углерод при тройной связи (алкины) |
=С= | 0 | алленовый углерод (центральный углерод в структурах типа >C=C=C<) |
=Cim | 2 | Углерод при двойной связи с азотом в имино-группе (С в >C=N-) |
CO | 2 | Карбонильная группа в молекулах альдегидов, кетонов, сложных эфиров, карбоновых кислот |
О | 2 | Кислород в простых эфирах, спиртах, а также некарбонильный кислородный атом в сложных эфирах, карбоновых кислотах и ангидридах карбоновых кислот |
N | 3 | Трехвалентный азот (амины) |
=Nim | 1 | Азот имино-группы (N в >C=N-) |
=Naz | 1 | Азот азо-группы (N в -N=N-) |
Nb | 0 | Ароматический азот (пиридин, пиразин и пиримидин, но не пиридазин) |
CS | 2 | Тиокарбонил |
S | 2 | Двухвалентная сера (сульфиды) |
SO2 | 2 | Группа сульфонов |
SO | 2 | Сульфоксидная группа |
1-Ad | 1 | 1-Адамантильный фрагмент |
Подобные работы: