Дифференциальный диагноз при ожирении
II. ЗНАЧЕНИЕ ИЗУЧАЕМОЙ ТЕМЫ.
Ожирение в настоящее время имеет не только медицинское, но и социальное значение, так как является благоприятной почвой для возникновения и прогрессирования наиболее распространенных заболеваний—атеросклероза и ишемической болезни сердца, сахарного диабета, гипертонической болезни и многих других, возникающих у тучных лиц в 2—3 раза чаще, отягощает их течение, приводит к ранней инвалидности и смерти (смертность от различных заболеваний у лиц, страдающих ожирением, в 1,5—3 раза выше). Профилактика многих заболеваний сводится в первую очередь к профилактике и лечению ожирения. Распространенность ожирения весьма велика, составляет 20— 30 % среди всего населения и значительно увеличивается у лиц старше 40 лет. Все это свидетельствует о необходимости своевременного выявления лиц, страдающих ожирением, и активного их оздоровления, что особенно актуально в условиях всеобщей диспансеризации населения.
III. ЦЕЛЬ ЗАНЯТИЯ:
Общая: уметь диагностировать различные клинико-патогенетические формы ожирения, определять его степень и назначать лечение.
Конкретные:
1. Произвести антропометрическое измерение, определить степень ожирения у обследуемых больных.
2. Определить объем необходимого инструментального, рентгенологического и биохимического исследования, оценить их результаты.
3. Выявить у больных ожирением симптомы, свидетельствующие о патологии гипоталамуса, гипофиза и других эндокринных желез, определить форму ожирения.
4. Рассчитать диету в зависимости от профессии, энерготрат, возраста и степени ожирения больного. Дать конкретные рекомендации по диетическому питанию, использованию разгрузочных дней.
5. Определить показания к назначению анорексигенных препаратов.
6. Назначить патогенетическую лекарственную терапию в зависимости от формы эндокринно-метаболического ожирения.
7. Определить показания и назначить противовоспалительную, рассасывающую, десенсибилизирующую терапию при гипоталамическом ожирении.
8. Дать больному конкретные рекомендации по использованию физической нагрузки в лечении ожирения в зависимости от состояния его здоровья.
IV. ПЛАН ИЗУЧЕНИЯ ТЕМЫ
Самостоятельная работа:
Теоретическая подготовка:
Практическая работа:
Решение задач:
Подведение итогов:
Задание на следующее занятие:
V. САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ.
А. Вопросы базовых дисциплин, необходимых для усвоения данной темы:
Физиология и патофизиология липидного обмена.
Биохимия липидного обмена.
Анатомия и физиология гипоталамуса и его роль в регуляции аппетита, чувства насыщения и обмена веществ.
Акушерская патология. Особенности течения беременности и родов при ожирении.
Физиотерапия. Санаторно-курортное лечение при ожирении.
Б. Задания на проверку и коррекцию исходного уровня знаний:
Объясните на основании сведений, полученных при изучении
нормальной физиологии:
Какова роль гипоталамуса в регуляции обмена веществ, суточного ритма, терморегуляции.
Какова специфика действия гормонов передней и задней долей гипофиза.
Механизм взаимодействия гипоталамо-гипофизарной и периферической эндокринных систем.
Какова роль адренергической, допасинергической, серотонинергической систем и эндорфинов в регуляции жирового обмена.
Объясните на основании сведений, полученных при изучении
патологичуской анатомии и физиологии:
Роль гипоталамуса в патогенезе алиментарно-конституционального и гипоталамического ожирения.
Ожирение как предиабет. Патогенез нарушения толерантности к глюкозе при ожирении.
Дефицит тиреоидных гормонов как фактор нарушения жирового обмена.
Причины гиперэстрогенемии и ее роль в патологии гипоталамо-гипофизарно-половой системы.
Причины андрогенизации и развитие вторичного склерокистоза яичников.
Задачи для самопроверки:
Укажите, какие из перечисленных гормонов оказывают:
а) липогенетическое;
б) липолитическое;
в) антилиполитическое действие;
г) существенно не влияют на липидный обмен:
1.1. Катехоламины. 1.2. Гликокортикоиды. 1.3. Андрогены надпочечников.
Минералокортикоиды. 1.5. Тиреоидные гормоны. 1.6. Глюкагон.
1.7. Половые гормоны. 1.8. Пролактин. 1.9. Кортикотропин.
1.10. Соматотропин. 1.11. Гонадотропин. 1.12. Тиротропин.
1.13. Меланотропин. 1.14. Липотропин.
Укажите, какие из перечисленных факторов влияют на аппетит:
2.1. Эмоциональный фактор.
2.2. Уровень глюкозы в крови.
2.3. Рефлекторное возбуждение рецепторов полости рта и желудка.
2.4. Состояние вентролатеральных ядер гипоталамуса.
2.5. Состояние вентромедиальных ядер гипоталамуса.
2.6. Все перечисленные факторы.
Определите, какие из указанных факторов вызывают гипоталамические нарушения чувства насыщения:
3.1. Психическая травма.
3.2. Физическая травма.
3.3. Инфекция.
3.4. Прием лекарственных средств.
3.5. Заболевания наружных половых органов.
3.6. Все перечисленные факторы.
Литература:
Холодова Е.А. Справочник по клинической эндокринологии. Минск 1996 г.
Старкова Н. Т. Клиническая эндокринология. М 1991 г.
Френкель И.Д., Першин С.Б. сахарный диабет и ожирение. М. 1996 г.
Бондар П.Н., Зелинский Б.А., Руководство к практическим занятиям по эндокринологии. Киев. 1989г.
В. Структура содержания темы
Определение.
Классификация форм ожирения.
Расчет степени тяжести ожирения.
Этиопатогенез каждой из форм ожирения.
Клиническая картина.
Дифференциальная диагностика.
Лечение.
ОЖИРЕНИЕ
Состояние, сопровождающееся избыточным накоплением жировой ткани в организме и приводящее к увеличению нормальной массы тела на 20% и более на фоне активации липосинтеза и угнетения липолиза.
Классификация.
В клинической практике принято выделять следующие формы ожирения:
1. Алиментарную.
2. Эндокринную.
3. Церебральную.
4. Лекарственную.
1. Алиментарные формы — привычно-гипералиментарное дезрегуляционное, конституционально - наследственное, смешанное.
2. Эндокринные формы — болезнь и синдром Иценко - Кушинга, гипотиреоз, гипо-питуитаризм, гипогонадизм, гиперинсулинизм.
3. Церебральные формы — корковые, гипоталамо-гипофизарные, гипоталамические, посттравматические, постинфекционные, опухолевые и вследствие повышения внутричерепного давления.
Лекарственные формы ожирения вызываются передозировкой инсулина, фенотиазидами, глюкокортикоидами, ципрогептадином, антидепрессантами.
По типу распределения жировой ткани в организме выделяют:
андроидный,
гиноидный,
смешанный виды ожирения.
Первый отличается отложением жировой ткани преимущественно в верхней части туловища, при гиноидном — жир скапливается в основном в нижней части тела и при смешанном типе происходит относительно равномерное распределение подкожножировой клетчатки. Выявлена зависимость между характером распределения жировой ткани и наличием метаболических осложнений. В частности, андроидный тип ожирения чаще, чем другие, сочетается с нарушенной толерантностью к глюкозе или с диабетом, гипертонией, гиперлипидемией, гиперандрогенией и гирсутизмом у женщин.
Поморфологическим изменениям жировой тканивыделяют:
а) гипертрофическое (увеличение массы каждого адипоцита) ожирение;
б) гиперпластическое (увеличение количества адипоцитов) ожирение.
Гипертрофический тип ожирения, характерный для заболевания, проявившегося в зрелом возрасте. Гиперпластическое или смешанное ожирение (сочетание гипертрофии и гиперплазии адипоцитов) отмечается у лиц с избыточной массой тела с детства. Уменьшение количества жировой ткани у тучных сопровождается изменением только размеров жировых клеток, число же их остается практически постоянным, даже в условиях резкого похудания. Этим объясняется резистентность к снижению веса при гиперпластическом и смешанном типах ожирения и важность профилактики заболевания с раннего детского возраста.
По степеням ожирения выделяют:
1 степень — избыточный вес превышает нормальную массу тела на 10—29 %.
II степень — избыточный вес превышает нормальную массу тела на 30—49 °о.
III степень — избыточный вес превышает нормальную массу тела на 50—99 %.
IV степень— вес тела избыточен более чем на 100%.
Похарактеру течения заболевание классифицируют как стабильное или прогрессирующее.
Наиболее адекватным значением, характеризующим ожирение, является
индекс массы тела, вычисляемый по формуле: масса тела в кг/рост в м2.
За норму принимается индекс массы, соответствующий 20—24,9.
Для определения нормальной массы тела используют таблицы для определения идеальной массы тела с учетом роста, пола, возраста и типа конституции. Кроме того, для определения нормальной массы тела может быть применен ряд индексов:
Индекс Брока используется при росте 155—170 см. Нормальная масса тела при этом равняется (рост (см) - 100 ) – 10 (15%).
Индекс Брейтмана. Нормальная масса тела рассчитывается по формуле — рост (см) 0,7 — 50 г.
Индекс Борнгардта. Идеальная масса тела высчитывается по формуле — рост (см) окружность грудной клетки (см) /240.
Индекс Давенпорта. Вес человека (г), делится на рост (см), возведенный в квадрат. Превышение показателя выше 3,0 свидетельствует о наличии ожирения.
Индекс Одера. Нормальная масса тела равна расстоянию от темени до симфиза (см) 2 - 100.
Индекс Ноордена. Нормальный вес равен рост (см) 420/1000.
Индекс Татоня. Нормальная масса тела =
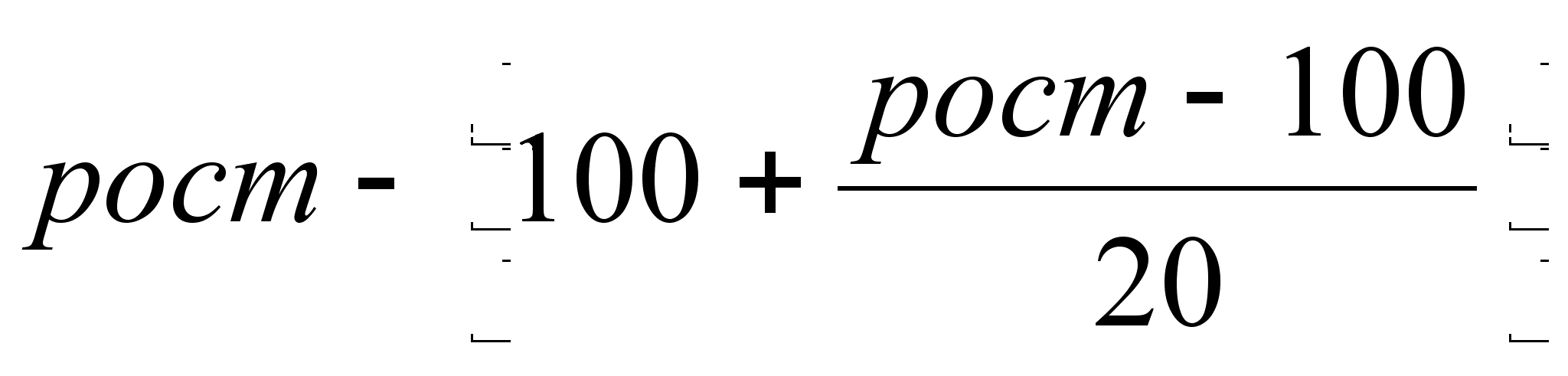 .
.
В клинической практике наиболее часто используется для оценки массы тела индекс Брока.
Кроме росто-весовых показателей может быть использован метод определения кожной складки, предложенный Коровиным. По этой методике определяется толщина кожной складки в подложечной области (в норме —1,1— 1,5 см). Увеличение толщины складки до 2 см свидетельствует о наличии ожирения.
Этиология и патогенез.
Согласно рассмотренной выше классификации, существует 4 различные этиопатогенетические формы ожирения:
I форма —это экзогенно-конституциональное, или алиментарное, ожирение.
Этиологические факторы, вызывающие развитие этой формы ожирения, подразделяют на экзогенные и эндогенные.
К экзогенным факторам относят: доступность еды и переедание с раннего детства; рефлексы, связанные со временем и количеством еды; усвоенные типы питания (национальные традиции); гиподинамия.
Эндогенные факторы, способствующие развитию ожирения, следующие: предрасполагающая к ожирению наследственность; конституция жировой ткани; активность жирового обмена; состояние гипоталамических центров сытости и аппетита; дисгормональные состояния. Именно дисгормональные состояния (беременность, роды, лактация, климакс) часто являются предрасполагающими к развитию ожирения.
Избыточное потребление пищи сопровождается частым повышением глюкозы крови и способствует развитию гиперинсулинизма. В свою очередь, гиперинсулинизм стимулирует аппетит, замыкая порочный круг, и одновременно способствует активации липосинтеза. Кроме того, известно, что формирование чувства голода и насыщения зависит от активности гипоталамических центров, расположенных в вентролатеральном (центр сытости) и вентромедиальном (центр голода) ядрах гипоталамуса. Активность «центра голода» модулируется допасинергической системой, а «центра сытости» — адренергической системой. Доказано влияние эндорфинов и серотонинергической иннервации на регуляцию и формирование массы тела. Кроме того, известно, что в регуляции аппетита принимают участие пептиды желудочно-кишечного тракта (холецистокинин, субстанцйя Р, опиоиды, сомато-статин, глюкагон), являющиеся периферическми медиаторами насыщения, а также нейропептиды и моноамины центральной нервной системы. Последние влияют на количество потребляемой пищи, продолжительность еды, определяют пищевые наклонности. Одни (опиоидные пептиды: рилизинг-фактор гормона роста, норадреналин, -аминомасляная кислота) увеличивают, другие (холецистокинин, кортикотропин-рилизинг фактор, допамин, серотонин) снижают потребление пищи.
II форма — эндокринные формы ожирения
Эндокринное ожирение является симптомом первичной патологии эндокринных желез (гиперкортицизм, гипотиреоз, гипогонадизм, инсулинома). И хотя при всех этих формах имеются различной степени выраженности гипоталамические нарушения (первичные или вторичные), сопровождающиеся избыточным липогенезом, они имеют отдельные этиологические формы с нарушениями в определенных звеньях нейроэндокринной системы.
Гипоталамо-гипофизарно-тиреоидная система.
Некоторые авторы отмечают изменение чувствительности периферических тканей (наличие резистентности) к тиреоидным гормонам вследствие уменьшения рецепторных мест. Сообщается также о нарушении в некоторых случаях связывания Т4 тироксинсвязывающим глобулином, усилении распада Т4, приводящих к снижению содержания тироксина и соответственно трийодтиронина в тканях, развитию относительной тиреоидной недостаточности и появлению клинических признаков гипотиреоза у таких больных.
Отмечается снижение продукции гипофизарного тиротропина и его реакции на стимуляцию тиролиберином. Снижение продукции тиротропина, вероятно, обусловлено гиперсекрецией соматостатина, обладающего тропностью к клеткам, продуцирующим тиреотропин, и уменьшением количества свободных рецепторов к тиролиберину. Отмечается инверсия суточного ритма секреции гормонов. В результате снижения секреции тиреотропина возможно развитие вторичного, чаще субклинического, гипотиреоза, сопровождающегося снижением уровней трийодтиронина и тироксина. В свою очередь, снижение функции щитовидной железы способствует прогрессированию ожирения из-за уменьшения основного обмена и активации липогенеза. При исследовании и трактовке результатов уровней тироксина и трийодтиронина следует иметь в виду, что при голодании или резком ограничении калорийности рациона (особенно за счет ограничения углеводов) уровень гормонов может достоверно снижаться. Эти колебания в уровнях гормонов являются чаще всего следствием нарушений периферической их конверсии и носят компенсаторный характер.
Гипоталамо-гипофизарно-надпочечниковая система.
Известно, что изменения гипоталамо-гипофизарно-надпочечниковой (ГГН) системы являются одной из причин развития гиперинсулинемии, нарушения толерантности глюкозы, дислипидемии и артериальной гипертензии. Модель поведения человека, которая включает употребление алкоголя, курение, стрессовые ситуации и чрезмерную физическую нагрузку, может сенсибилизировать ГГН систему и влиять на распределение жира в организме.
Так, при абдоминальном распределении жировой ткани отмечается высокий риск сердечно-сосудистых заболеваний. Для измерения этого распределения использовали индекс ОТ/ОБ.
Соотношение окружности талии к окружности бедер (ОТ/ОБ) — простой метод, наиболее часто используемый при определении количественного распределения жировой ткани. Высокое значение индекса ОТ/ОБ означает преимущественное расположение жировой ткани в абдоминальной области. Термины "ожирение верхнего типа" и "абдоминальное ожирение" часто используются как синонимы при диагностике больных с повышенным ОТ/ОБ. Мужчины и женщины входят в группу риска если индекс ОТ/ОБ больше или равен 0,90 и 0,80 соответственно.
Существует связь между региональным распределением жировой ткани и нарушениями в глюкозо-инсулиновом метаболизме. Отмечены высокая частота развития сахарного диабета и нарушения толерантности глюкозы у женщин с "верхним типом ожирения" в сравнении с "нижним типом ожирения". Таким образом характер распределения жира гораздо важнее, чем сам факт ожирения. Адипоциты различны в зависимости от места их нахождения. Адипоциты висцеральной жировой ткани метаболически более активны и легко высвобождают свободные жирные кислоты (СЖК) в ответ на любую липолитическую стимуляцию. СЖК из висцеральных адипоцитов попадают непосредственно в портальную систему кровообращения. Высокая концентрация СЖК ингибирует связывание и захват инсулина гепатоцитами, снижает утилизацию глюкозы в цикле глюкоза – жирная кислота, что приводит к снижению толерантности к глюкозе и системной гиперинсулинемии.
Кроме того при висцеральном ожирении активность плазменной постгепариновой липопротеиновой липазы снижается, в то время как активность гепатической триглицеридной липазы повышается, что способствует уменьшению продукции предшественников ЛВП, высокому уровню триглицеридов и ЛНП в плазме.
Доказано, что абдоминальное ожирение способствует развитию АГ. Возможные связи между гиперинсулинемией и артериальной гипертензией:
Увеличение почечной канальцевой реабсорбции натрия
Увеличение активности симпатической нервной системы
Пролиферация гладкомышечных клеток сосудов и фибробластов – атеросклероз.
При нарушениях в эндокринной регуляции ГГН системы наблюдается достоверное повышение секреции кортикотропина и нарушение его суточного ритма (нет снижения в дневное и вечернее время) параллельно увеличению степени ожирения. При этом отмечается нарушение механизма обратной связи, которое выявляется при проведении дексаметазоновой пробы в различное время суток. У большого числа больных (особенно с ожирением III—IV степени) увеличена скорость продукции кортизола, ускорен его метаболизм, повышена экскреция 17-оксикортикостероидов с мочой. Уровень же кортизола в плазме остается в норме. Повышение скорости метаболического клиренса кортизола приводит к уменьшению его содержания в плазме и через механизм обратной связи стимулирует секрецию актг. В свою очередь повышение скорости секреции АКТГ ведет к увеличению продукции кортизола, и таким образом его уровень в плазме поддерживается в нормальных пределах. Повышение секреции кортикотропина обусловливает также ускорение продукции андрогенов надпочечниками. При развитии выраженного ожирения (III—IV ст.) часто отмечается гиперинсулинизм, вызывающий частые бессимптомные гипогликемические реакции, которые способствуют активации продукции гликокортикоидов (в числе других контринсулярных гормонов). Избыточная секреция кортикотропина стимулирует продукцию андрогенов надпочечниками, что сопровождается симптомами маскулинизации у женщин (гирсутизм, дис- или аменорея и т. д.), и минералокортикоидов (альдостерона, который усугубляет артериальную гипертензию, часто сопутствующую ожирению).
Гипоталамо-гипофизарно-половая система.
Ведущий механизм гипоталамо-гипофизарно-гонадальных нарушений — нарушение гипоталамического контроля за продукцией фолли- и лютропина, что было доказано при использовании различных фармакодиагностических проб (в частности, с люлиберином, сульпиридом, рифатиронином). Базальные же уровни гонадотропинов достоверно не отличаются от нормальных значений. Наблюдаемые у подавляющего большинства рассматриваемых больных нарушения половой функции (у женщин в виде нарушений фертильности, у мужчин — нарушений потенции) являются результатом нарушения секреции, инактивации и связывания с белками плазмы половых гормонов. В жировой ткани активируется ароматизация андрогенов с их превращением в эстрогены (эстрадиол и эстрон). У мужчин с ожирением III—IV степени отмечается снижение уровня тестостерона, вначале без нарушения вторичных половых признаков. Однако наблюдающаяся активация периферической конверсии тестостерона в эстрадиол и андростендиола в эстрон способствует нарастанию гиперэстрогенемии и последующему развитию гинекомастии (чаще ложной). Центральные нарушения секреции гонадотропинов приводят к постепенному появлению гипогонадотропного гипогонадизма. Гиперэстрогенемия может являться предрасполагающим фактором для развития карцином эндометрия. У девочек-подростков ожирение оказывает влияние на сроки появления менархе. Менархе наступает у девочки после достижения ею «критической» массы тела, составляющей 48 кг. Так, полные девочки скорее набирают «критическую» массу, и менархе у них наступает раньше, хотя менструации долго носят нерегулярный характер.
У некоторых женщин с ожирением отмечается неадекватная продукция прогестерона в лютеиновую фазу менструального цикла, что тоже может быть причиной нарушения их фертильности. По законам обратной связи периферическое нарушение в секреции половых гормонов приводит к вторичным нарушениям гипоталамо-гипофизарной секреции.
Кроме того, у женщин с ожирением возможно развитие вторичного склерокистоза яичников с развитием андрогенизации. Андрогенизация является следствием ускорения превращения андростендиола в тестостерон и эстрон. Эстрон вызывает сенсибилизацию гипофиза к люлиберину и последующую монотонную гиперсекрецию лютропина (без овуляторного пика). Избыток лютропина стимулирует гиперплазию стромы яичника и увеличивает синтез андрогенов. Кроме того, на фоне ановуляторных циклов гранулезные клетки не вызревают и являются источником продукции андрогенов.
Поджелудочная железа.
В генезе гиперинсулинемии при ожирении имеют значение нарушения гипоталамической регуляции, реализуемые через симпатическую и парасимпатическую нервную систему, опиоидные пептиды, желудочно-кишечные гормоны, в частности желудочный тормозящий полипептид, особенности питания.
В основе инсулинорезистентности лежит снижение чувствительности к инсулину на всех изучаемых метаболических путях, начиная со связывания его рецепторами. Предполагают, что при ожирении уменьшается число рецепторов к инсулину на поверхности эффекторных клеток, приводящее к снижению связывания и тем самым уменьшению специфического эффекта этого гормона.
Гиперсекреция инсулина, как уже указывалось, является характерным признаком ожирения. Гиперинсулинизм стимулирует аппетит и одновременно процессы липогенеза. Указанные факторы, в свою очередь, являются факторами риска развития сахарного диабета II типа. Несмотря на гиперинсулинизм, уровень глюкозы крови не бывает снижен, что может быть объяснено резистентностью рецепторов к инсулину или уменьшением количества рецепторов инсулина на поверхности адипоцитов. Одновременно с продукцией избыточного количества инсулина отмечается избыточное образование С-пептида и проинсулина.
Секреция глюкагона снижается, даже субклинические гипогликемические реакции не сопровождаются избыточной продукцией глюкагона.
Гастроинтестинальные пептиды, в их числе панкреатический полипептид, являются, как известно, ингибиторами аппетита, оказывающими свое влияние посредством воздействия на глюкозозависимую секрецию инсулина. Аналогичным действием обладают желудочный ингибиторный полипептид, гастрин, секретин, холецистокинин, вазоактивный интестинальный пептид.
Кроме того, при ожирении наблюдается угнетение синтеза и секреции соматотропина вследствие активации образования соматостатина.
III форма церебрального ожирения может быть вызвана травмами черепа, нейроинфекциями, опухолями мозга или длительным повышением внутричерепного давления.
IV форма лекарственногоожирения формируется при длительном приеме препаратов, повышающих аппетит или активирующих липосинтез.
Патогенез ожирения зависит от классификационной формы заболевания. Однако, независимо от формы ожирения, оно является результатом переедания (т. е. потребления пищи, превышающего необходимые энергетические траты у конкретного индивидуума).
Патогенез ожирения представлен на схеме 1. и 2.
СХЕМА ПАТОГЕНЕЗА ОЖИРЕНИЯ
Вентромедиальные и вентролатеральные ядра гипоталамуса с центрами голода и аппетита (-эндорфин)
Нарушение функции гипофиза СТГ, липотропин
Нарушение функции щитовидной железы, надпочечников, гонад
Переедание и гиподинамия
Ожирение
Наследственность и конституция
Поджелудочная железа
Инсулин
Глюкагон
Адипоциты. Инфильтрация
печени.
НЭЖК, триглицеридов, -липопротеидов
Гиперкоагуляционный синдром


СХЕМА 1
ОЖИРЕНИЕ
Переедание,
Гиподинамия,
Наследственность
Активность
гипоталамических центров
Опухоль мозга, повышение ВЧД
Травмы,
Инфекции,
Интоксикации
Эндокринные заболевания, Нарушение регуляции обмена веществ
веществ
Активация центра голода, липосинтеза,
Этиология
Патология гипоталамуса, Переедание
Конституциональные и обменные, генетически обусловленные нарушения
Корково-церебральные нарушения
Патогенез
Нарушение энергетического баланса (преобладание липогенеза над липолизом)
Клинические проявления
Увеличение массы тела
Нарушения функции нервной системы
Нарушения кровообращения дыхания, пищеварения,мочевыделения
Нарушения функции опорно-двигательного аппарата
Эндокринно-метаболическое нарушения
Дифференциальная диагностика
Обоснование диагноза
Лечение
Гипоталамо-гипофизарное, эндокринно-метаболическое, церебральное ожирение
Увеличение массы тела более должной на 20%
Диета
Патогенетическое
Физические упражнения, занятия спортом
Симптоматическое
Алиментарная
Церебральная
Эндокринная
Формы
Лекарственная
Эндокринные нарушения
СХЕМА 2.
Клиническая картина
Ожирение, независимо от его причин, сопровождается вторичными изменениями во многих внутренних органах. В начальных стадиях ожирения сохраняются функциональные и адаптационные свойства организма (кроме наличия избыточной массы тела, никаких других характерных симптомов у этой категории больных не выявляется). Это так называемое компенсированное ожирение. При прогрессировании ожирения наблюдается переход его в «декомпенсированное» ожирение с развитием, как правило, синдрома хронической недостаточности отдельных органов или систем. Особенно трудно разграничить ожирение как причину заболевания и ожирение как сопутствующий основному заболеванию синдром.
Трофические нарушения.
У больных с ожирением появляется склонность к вторичным воспалительным процессам (фолликулиты, упорный фурункулез, флегмоны, микозные поражения кожи и ее придатков, экземы). У многих больных эти проявления сочетаются с симптомами нарушения трофики кожи (цианоз, выпадение волос, повышенная ломкость ногтей и т.д.). Особого внимания заслуживает появление на теле больных полос растяжения. Вначале они имеют телесно-розовый цвет, впоследствии приобретают серо-желтую окраску. (Исключение составляют багрово-цианотичные стрии, появляющиеся на теле при гиперкортицизме.) Расположение полос обычно симметричное, в местах максимального скопления жировой ткани (живот, бедра, ягодицы, грудные железы). В появлении полос растяжения имеет значение механический фактор перерастяжения кожи и трофический фактор, обусловливающий нарушения белкового обмена (снижается образование коллагена). В результате снижения эластичности кожи и ослабления мышечного тонуса могут появляться грыжевые выпячивания (пупочные, паховые, бедренные), расхождение прямых мышц живота. Кроме того, у больных отмечаются изменения сосудистой системы кожи, которые проявляются в виде телеантиэктазий. Характерным признаком ожирения является лимфостаз нижних конечностей.
Изменения костно-суставной системы.
Избыточная масса тела оказывает чрезмерную нагрузку на опорно-двигательный аппарат и способствует развитию в нем различных дегенеративных процессов, ограничивающих двигательную функцию больного. В свою очередь, ограничение двигательной активности больных усугубляет прогрессирование ожирения. Наличие жалоб на боль в суставах, пояснице указывает на поражение костей, что подтверждается болезненностью при пальпации поперечных отростков шейных, грудных и поясничных позвонков, исчезновением физиологического изгиба позвоночника, ограничением его подвижности (грудной, шейный лордоз, спондилоартроз, вторичный радикулит). Характерные изменения костно-суставной системы следующие:
1. Дегенеративные изменения в суставах позвоночника и конечностей с развитием деформирующего спондилеза или остеоартроза крупных суставов.
2. Системный остеопороз.
Вальгусные деформации стоп и колен, плоскостопие.
Отмечается повышенная склонность к кариозным процессам. Кроме того, достоверно у больных увеличение частоты альвеолярной пиореи, парадонтоза.
Изменения в органах пищеварительного такта.
Со стороны пищевода, желудка, тонкого кишечника не выявлено каких-то достоверных функциональных отклонений. Нередко наблюдается растяжение и опущение желудка, обусловленное частым поступлением в него большого количества пищи (механический фактор).
Нарушение функции кишечника заключается в основном в нарушении его моторики вследствие малоподвижного образа жизни, слабости мышц брюшного пресса, гипотонии мышц кишечной стенки и избыточном отложении жира в области брыжейки и сальника. Клинически эти нарушения проявляются атоническими запорами, чрезмерным газообразованием, разлитыми болевыми ощущениями в области живота. Вздутие живота сопровождается развитием венозного застоя, что наиболее типично выявляется в виде варикозного расширения геморроидальных вен. В свою очередь, геморрой способствует дисфункции прямой кишки (возможно появление кровоточащего геморроя, трещин ануса, рефлекторных запоров).
Четкие изменения прослеживаются со стороны печени и желчных путей. При прогрессировании ожирения прямо пропорционально увеличивается масса печени за счет ее жировой инфильтрации, отмечается отложение жира в воротах, в капсуле печени, в междолевых пространствах, в самом гепатоците, в клетках ретикулоэндотелиальной системы печени и прогрессирующее снижение в ней количества гликогена. Эти изменения вызывают нарушения функции печени, проявляющиеся чувством тяжести в правом подреберье, снижением переносимости глюкозы, склонностью к кетонообразованию, повышенным образованием холестерина. Метаболизм желчных пигментов и ферментообразо-вательная функция не страдают.
Не вызывает сомнения, что ожирение является фактором, предрасполагающим к развитию заболеваний желчевыводящих путей, таких как желчно-каменная болезнь, холецистит, дискинезия желчевыводящих путей. В основе этих процессов лежат дискинезия, способствующая застою желчи; снижение неспецифической резистентности ожирелых людей и изменение коллоидных свойств желчи за счет повышенного в ней содержания холестерина и других веществ. Желчно-каменная болезнь протекает с очень скудной симптоматикой и поэтому часто диагностируется с опозданием.
Не вызывает сомнения, что различные клинические формы панкреатита чаще встречаются на фоне ожирения. При этом отмечается снижение активности внешнесекреторной части поджелудочной железы (со снижением активности и количества амилазы, липазы, трипсина) и нарушение ее внутрисекреторной функции с развитием нарушенной толерантности к глюкозе или сахарного диабета II типа.
Сердечно-сосудистые поражения у больных ожирением встречаются в виде ишемической болезни сердца, системного атеросклероза, недостаточности венозного кровообращения в нижних конечностях, миокардиодистрофии, артериальной гипертензии. Наиболее специфическим из данного перечня патологических процессов является миокардиодистрофия. При этом увеличивается количество жировой ткани вне перикарда (в области правого желудочка и верхушки сердца), между волокнами миокарда, в самих миокардиальных клетках. Увеличение массы сердца сопровождается его гипертрофией. Следует отметить, что у здоровых лиц существует пропорциональная зависимость между массой сердечной мышцы и массой тела, тогда как у ожирелых людей увеличение массы миокарда, емкость сердца и степень его гипертрофии отстают от нарастания массы тела.
Обильная васкуляризация жировой ткани приводит к повышенному потреблению кислорода, что требует компенсаторного увеличения минутного объема сердца.
Увеличение ударного объема сердца в этой ситуации недостаточно, поэтому возрастает частота сердечных сокращений в покое и при физической нагрузке. Эти явления могут быть причиной снижения резервных возможностей миокарда, что приводит к недостаточности кровообращения. Указанные гемодинамические изменения сопровождаются утомляемостью, сердцебиениями, одышкой даже при небольших физических нагрузках, стенокардическими болями в области сердца. При перкуссии определяе